Содержание
Оценка количества слабосвязанных белков стержня волоса при алопеции
Изменение функциональной активности волосяных фолликулов и нарушение цикла их развития может привести к выпадению волос (алопеции). Однако вопрос о существовании прямой связи между функциональной активностью волосяных фолликулов и качеством формируемого ими волоса практически не изучен.
Стержень волоса на 80% состоит из белков (кератинов). Высокомолекулярные кератины (так называемые тяжелые, молекулярная масса которых превышает 20 кД) обладают низкой растворимостью и образуют фибриллы, находящиеся в слое кортекса. Они окружены матриксом, состоящим из легких низкомолекулярных кератинов с молекулярной массой 6—20 кД. Легкие кератины растворимы в воде и при повреждении кутикулы волоса или при ослаблении связей с другими белками кортекса могут вымываться из стержня волоса. Показано, что вымывание белков усиливается при повреждении кутикулы в результате отбеливания и химической завивки [1, 2]. В свою очередь повреждение кутикулы может открывать внешним воздействиям более глубокие слои стержня волоса, что ведет к дальнейшему ослаблению связей между белками кортекса [3].
Это означает, что усиление процесса вымывания белков из волоса может отражать не только внешние повреждения, затрагивающие кутикулу, но и изменение структуры кортекса, прежде всего увеличение содержания слабосвязанных белков [1]. Такие слабосвязанные белки постепенно вымываются из стержня волоса, а при механической гомогенизации волоса в водной среде переходят в раствор (растворимые белки).
Остается неизвестным, зависит ли увеличение содержания слабосвязанных белков только от внешних воздействий или может быть следствием нарушения функциональной активности волосяных фолликулов при алопеции.
Цель работы — оценка количества слабосвязанных белков волос пациентов с андрогензависимой алопецией (АГА) и телогеновым выпадением (ТВ) волос. В работе оценивали скорость вымывания белков из стержня волоса в стандартных условиях. Результаты сопоставляли с данными для здоровых добровольцев. Затем волосы подвергали механической дезинтеграции в водной среде и оценивали содержание растворимых белков. Материал для исследований (волосы) брали с теменной и затылочной зоны волосистой части головы.
Материал для исследований (волосы) брали с теменной и затылочной зоны волосистой части головы.
Материал и методы
Измерение поглощения света проводили на спектрофотометре Shimadzu UV-1700, флюоресценцию проб измеряли на спектрофлюориметре Hitachi F 4000.
Использовали следующие реактивы: бычий сывороточный альбумин (БСА; «Sigma»), кератин из эпидермиса человека («Sigma»), L-триптофан («Calbiochem»), карбонатный буферный раствор 0,1 М, рН 10,2.
Объектом исследований служили волосы пациентов с АГА (20 человек, из них 2 мужчины; возраст 35±10 лет) и ТВ (46 человек, из них 3 мужчины; возраст 33±9 лет), а также здоровых добровольцев (ЗД) — лиц без трихологической патологии (30 человек, из них 5 мужчин; возраст 26±12 лет).
Волосы извлекали с помощью пинцета из зоны темени и затылка. Материал помещали в отдельные герметичные пластиковые пакеты и хранили при 8 °С.
Получение проб вымываемого белка
Вымывание белка проводили следующим образом: фрагменты волос длиной около 10 мм взвешивали и помещали в карбонатный буферный раствор (0,1 М, рН 10,2) так, чтобы соотношение массы волос и буферного раствора составляло 1:250.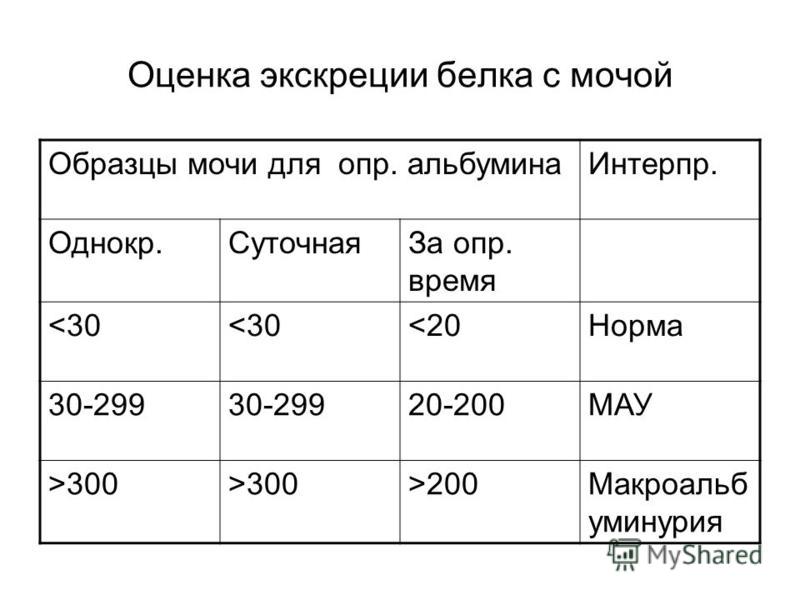 Инкубировали пробы при комнатной температуре в течение 30 мин при постоянном мягком встряхивании. Отбирали жидкость и осаждали механические примеси центрифугированием при 900 об/мин в течение 15 мин. Полученные пробы вымываемого белка использовали для измерений.
Инкубировали пробы при комнатной температуре в течение 30 мин при постоянном мягком встряхивании. Отбирали жидкость и осаждали механические примеси центрифугированием при 900 об/мин в течение 15 мин. Полученные пробы вымываемого белка использовали для измерений.
Анализ динамики вымывания белков (рис. 1)Рисунок 1. Вымывание белка при инкубации волос ЗД в буферном растворе (рН 10,2) в зависимости от времени инкубации. Результаты представлены в пересчете на вес образца волос мг/г. Оценку белка проводили путем измерения поглощения проб при 240 нм. выявил линейную зависимость количества вымываемого белка от времени в выбранном диапазоне, поэтому содержание белка в пробе по окончании инкубации (30 мин) отражало скорость вымывания белка из стержня волоса (мг/г за 30 мин).
Получение проб растворимого белка
После получения вымываемого белка волосы помещали в ручной гомогенизатор Поттера и растирали до получения однородной суспензии в буферном растворе. Нерастворимую фракцию осаждали центрифугированием (900 об/мин, 30 мин). Отбирали прозрачный супернатант, содержащий растворимые белки.
Нерастворимую фракцию осаждали центрифугированием (900 об/мин, 30 мин). Отбирали прозрачный супернатант, содержащий растворимые белки.
Оценка содержания белка
Для оценки белка волос были опробованы три метода: биуретовый, Лоури и поглощение света в ультрафиолетовой части спектра.
Результаты пересчитывали на белковый эквивалент, используя в качестве стандарта БСА, и нормировали на вес пробы волос (мг белка/г волос).
Оценку белков в реакции с биуретовым реактивом проводили с использованием набора реактивов RANDOX (Великобритания), для метода Лоури применяли реактивы компании «Sigma». Биуретовый метод был принят в качестве референтного, поскольку его результаты почти не зависят от специфики исследуемого белка. Этот метод с успехом применялся при работе с большим количеством материала (20 мг в 1 мл буферной среды) [2].
Метод Лоури [4] также применялся для исследования вымываемых белков [3], однако и в этом случае вносили 10—15 мг волос в 1 мл водной среды.
В нашей работе при использовании метода Лоури получены значительно заниженные результаты по сравнению с биуретовым методом. Причина, по-видимому, заключается в том, что фенольный реактив Фолина реагирует с ароматическими аминокислотами белка, особенно с тирозином, а, по нашим данным, в экстрактах волос молярная доля тирозина мала.
Предложенный нами третий метод — поглощение света в области 240 нм — оказался чувствительнее к белку волос, чем биуретовый метод, и позволил проводить измерения в диапазоне 1—2 мг волос в 1 мл. Полученные нами спектры поглощения вымываемого белка (рис. 2),Рисунок 2. Спектры поглощения кератина (1), БСА (2), вымываемого белка волос ЗД (3). Концентрация кератина и БСА — 20 мкг/мл. Вымываемый белок получен при инкубации 5 мг волос донора в 1 мл карбонатного буферного раствора (30 мин при комнатной температуре) и разведен водой из расчета 1:5. Значения оптической плотности представлены за вычетом показателей для соответствующего разведения карбонатного буферного раствора. а также кератина и альбумина в диапазоне 220—300 нм обнаружили максимум поглощения всех исследованных образцов при длине волны 230 нм.
а также кератина и альбумина в диапазоне 220—300 нм обнаружили максимум поглощения всех исследованных образцов при длине волны 230 нм.
Для того чтобы избежать резких колебаний за счет случайных смещений пика поглощения, в дальнейшем измеряли поглощение при длине волны 240 нм.
При измерении растворимого белка волос ЗД биуретовым методом концентрация белка составила 9 мг/г волоса, метод Лоури — 0,9 мг/г, а по поглощению света — 10 мг/г, т.е. практически как при применении биуретового реактива.
Несмотря на обнаруженные расхождения между методом оценки белка по поглощению при длине волны 240 нм и методом Лоури, мы выявили линейную зависимость между данными обоих методов при анализе растворимого белка волос ЗД (рис. 3).Рисунок 3. Связь между количеством растворимого белка волос ЗД (n=4) по данным измерения поглощения при 240 нм и методом Лоури. Коэффициент корреляции r=0,9, вероятность отсутствия корреляции р<0,01. Этот результат подтверждает наше предположение о том, что природа расхождения результатов заключается в специфичности метода Лоури.
Оценка собственной флюоресценции слабосвязанных белков
Для оценки флюоресценции вымываемого белка пробу помещали в кювету с сечением 1×1 см и регистрировали спектр флюоресценции при длине волны возбуждения 290 нм.
Флюоресценция — чувствительный метод анализа белков, широко используемый при изучении внешних воздействий, прежде всего — ультрафиолетового излучения [5].
Результаты анализа спектров собственной флюоресценции вымываемых белков волоса и сопоставление их со спектрами кератина и триптофана (рис. 4)Рисунок 4. Спектры флюоресценции растворов кератина 0,05 мг/мл (1), триптофана 0,20 мг/мл (2) и типичные спектры флюоресценции вымываемых белков волос (тонкие точечные линии — 3, 4, 5, 6). Длина волны возбуждения 290 нм. подтверждают данные других исследователей о содержании в белках волоса не только триптофана, но и его производных (например, N-формилкинуренина [6]). Таким образом, метод позволяет регистрировать появление продуктов модификации триптофана для оценки свойств вымываемых и растворимых белков волос, но наличие нескольких пиков затрудняет их прямую количественную оценку.
Для оценки количества слабосвязанных белков нами был использован метод оценки поглощения света при длине волны 240 нм. Данные для пациентов и ЗД получены этим методом.
Статистическая обработка результатов.
Для обработки результатов использовали программу Statistica 6.0. Независимые выборки (межгрупповые сравнения) сравнивали по критерию Манна—Уитни, а для связанных переменных (сравнение между зонами скальпа) использовали критерий Уилкоксона. Достоверными считали различия при р<0,05.
Результаты и обсуждение
Задачей нашего исследования была оценка количества слабосвязанных белков, т.е. белков, вымываемых буферным раствором из стержня волоса за 30 мин (рис. 5, I)Рисунок 5. Схема анализа волос пациентов и здоровых добровольцев. и переходящих в буферный раствор при механической дезинтеграции волоса (рис. 5, II). Схема анализа представлена на рис. 5.
Такая схема анализа позволила сравнивать скорость вымывания белка между группами и зонами волосистой части головы в каждой группе (см. таблицу).
таблицу).
Обнаруженные различия можно было соотнести с количеством растворимого белка волоса, получаемого при его механическом разрушении.
Наибольшая скорость вымывания белка обнаружена у пациентов с АГА. В зоне темени значение данного показателя у этих пациентов достоверно отличалось от такового ЗД (p<0,01) и было больше, чем в зоне затылка у этих же пациентов (p<0,02).
Поскольку скорость вымывания белка может быть следствием изменения белкового профиля в кортексе волоса, согласно выбранной схеме анализа (см. рис. 4) измеряли количество растворимого белка после разрушения волоса.
Содержание растворимого белка в волосах, полученных с зоны темени, было выше, чем у ЗД (p<0,01) и в зоне затылка (p<0,05). Этот результат подтвердил закономерности, полученные при анализе скорости вымывания белка.
В целом увеличение скорости вымывания белка в зоне темени по сравнению с зоной затылка отмечалось у 70% с АГА, в 55% случаев значения показателя были выше верхней границы значений, полученных для ЗД. В зоне затылка обнаружилось увеличение количества слабосвязанных белков по сравнению с нормой, но оно выявлялось только после разрушения волос (растворимый белок, p<0,05).
В зоне затылка обнаружилось увеличение количества слабосвязанных белков по сравнению с нормой, но оно выявлялось только после разрушения волос (растворимый белок, p<0,05).
У пациентов с ТВ скорость вымывания белка превышала таковую у ЗД здоровых добровольцев преимущественно в зоне затылка (p<0,01), однако количество растворимого белка не отличалось от показателей, полученных у ЗД. Более того, содержание растворимого белка в волосах из зоны темени у этих пациентов было достоверно выше, чем в зоне затылка (p<0,05).
У ЗД достоверных различий между зонами ни при анализе скорости вымывания белка, ни при оценке растворимого белка не выявлено.
Механизмы выпадения волос при АГА и ТВ различаются. Общим является сокращение продолжительности цикла анагена у значительного количества волос с преждевременным наступлением стадии катагена и последующей стадии телогена. ТВ свойственно диффузное поредение, тогда как при андрогенетическом выпадении страдает андрогензависимая область скальпа — лоб, темя. Кроме того, причины ТВ могут быть разной природы (диета, стресс, реакция на лекарственные препараты), что обусловливает значительный разброс данных, поскольку перечисленные факторы по-разному влияют на содержание слабосвязанных белков в стержне волоса.
Кроме того, причины ТВ могут быть разной природы (диета, стресс, реакция на лекарственные препараты), что обусловливает значительный разброс данных, поскольку перечисленные факторы по-разному влияют на содержание слабосвязанных белков в стержне волоса.
По-видимому, при АГА механизм, связывающий процессы регуляции жизни фолликула и синтеза белка, является общим для большинства пациентов, что позволило выявить достоверные различия по сравнению с ЗД, а также между зоной облысения (темя) и нормального роста (затылок) при анализе слабосвязанных белков.
Полученные результаты позволяют сформулировать следующие положения.
В стержне волос имеются растворимые белки, слабо связанные между собой и механическим каркасом стержня.
Чувствительным и достаточно простым методом оценки количества растворимых (слабосвязанных) белков волос может служить анализ белка по поглощению света при длине волны 240 нм.
Среднее содержание слабосвязанных растворимых белков у ЗД оценено как 18±2 мг на 1 г волос. Различий в показателях для затылочной и теменной областями головы не отмечено.
Различий в показателях для затылочной и теменной областями головы не отмечено.
У пациентов с АГА по сравнению со ЗД наблюдается значительно (примерно в 2 раза) повышенный выход слабосвязанных белков в волосах зоны темени. Это увеличение регистрируется как при измерении скорости вымывания белков из волоса, так и при оценке количества растворимых белков после дезинтеграции волоса.
У пациентов с АГА наблюдается достоверное увеличение содержания слабосвязанных белков в волосах зоны темени по сравнению с волосами зоны затылка. Это различие обнаруживается как при измерении скорости вымывания белков, так и при оценке количества растворимых белков после дезинтеграции волоса.
У пациентов с ТВ волос обнаружено увеличение скорости вымывания белков в зоне затылка по сравнению со ЗД. При этом повышения содержания растворимых белков, измеренного после разрушения волоса, не наблюдалось.
При сравнении показателей между пациентами с АГА и ТВ по зонам волосистой части головы показано, что содержание слабосвязанных белков у пациентов с АГА в зоне темени было достоверно выше, чем у пациентов с ТВ. Это справедливо и в отношении скорости вымывания белков, и в отношении общего количества растворимых белков.
Это справедливо и в отношении скорости вымывания белков, и в отношении общего количества растворимых белков.
Оценка слабосвязанных белков волоса (скорости вымывания белков и общего количества растворимых белков) может быть полезным инструментом при анализе состояния волос пациентов с алопецией и для мониторинга лечения. Полученные результаты указывают на целесообразность использования при алопеции средств, укрепляющих стержень волоса.
об исследованиях структуры белка, их роли в понимании патогенеза болезней и важности разнообразного CV
— Дмитрий, вы, как я поняла, занимаетесь изучением белков. И начать я хотела бы совсем со школьных азов. Что такое белки?
— Белки, говоря формально, — это гетерополимеры. А полимеры — это длинные молекулы, собранные из каких-либо звеньев. Бывают гомополимеры, составленные из одинаковых звеньев (со школьной скамьи все помнят полистирол или полиэтилен), а бывают гетерополимеры — из разных. Белки состоят из 20 типов аминокислот, еще две используются в зависимости от контекста. На самом деле, аминокислот намного больше, но природа в белках использует лишь эти 20. Хотя если считать так называемые посттрансляционные модификации (ковалентные химические модификации белка после его синтеза на рибосоме — прим. авт.), их будет значительно больше.
Белки состоят из 20 типов аминокислот, еще две используются в зависимости от контекста. На самом деле, аминокислот намного больше, но природа в белках использует лишь эти 20. Хотя если считать так называемые посттрансляционные модификации (ковалентные химические модификации белка после его синтеза на рибосоме — прим. авт.), их будет значительно больше.
— Почему именно такое число?
— Таков генетический код. Его расшифровали в 1960-х годах и выяснили, что аминокислот 20. И столь потрясающая универсальность наблюдается у всех живых организмов — все они имеют один и тот же генетический код и набор аминокислот. Некоторые вариации генетического кода, конечно, существуют, но их всего около 15, и они незначительны. А полипептидов — астрономическое число. Но не все из них становятся белками, потому что белки обладают особым свойством — выполнять разные функции в организме.
— Чем же белок отличается от случайной полипептидной цепи?
— В ходе эволюции сложился такой порядок аминокислот, при котором конкретная белковая молекула определяет трехмерную форму белка. Эта форма стабильная и жесткая, поэтому она способна выполнять какие-то функции. Поясню: возьмем, например, ножницы. У них есть функция — резать. Почему они могут это делать? Во-первых, потому что они твердые, а во-вторых, потому что у них есть острые лезвия. Если бы у нас был кусок киселя даже в форме ножниц, ничего разрезать им мы бы не смогли. То же самое с белками: есть, к примеру, белки, которые разрезают другие молекулы (ДНК, РНК, другие белки). И для этого им нужна определенная жесткая форма. Этим белки и отличаются от случайных полипептидов.
Эта форма стабильная и жесткая, поэтому она способна выполнять какие-то функции. Поясню: возьмем, например, ножницы. У них есть функция — резать. Почему они могут это делать? Во-первых, потому что они твердые, а во-вторых, потому что у них есть острые лезвия. Если бы у нас был кусок киселя даже в форме ножниц, ничего разрезать им мы бы не смогли. То же самое с белками: есть, к примеру, белки, которые разрезают другие молекулы (ДНК, РНК, другие белки). И для этого им нужна определенная жесткая форма. Этим белки и отличаются от случайных полипептидов.
— Какие еще функции выполняют белки?
— Белки выполняют 99,9% функций в нашем организме, практически все, которые существуют. Одно из исключений — рибосомы, на которых производятся белковые цепи, согласно инструкции, записанной в матричной РНК. То же самое относится к рибозимам — молекулам РНК, которые также способны сворачиваться в строго определенную трехмерную форму и выполнять свои задачи.
В целом, функции белков можно разложить по нескольким категориям. Одна из них — гормональная. За нее отвечает, например, такой известный белок, как инсулин. Инсулин — это первый белок, у которого была определена последовательность аминокислот. Это сделал Фредерик Сенгер, за что и получил первую Нобелевскую премию.
Одна из них — гормональная. За нее отвечает, например, такой известный белок, как инсулин. Инсулин — это первый белок, у которого была определена последовательность аминокислот. Это сделал Фредерик Сенгер, за что и получил первую Нобелевскую премию.
Еще одна функция — транспортная. Ею занимается, скажем, гемоглобин, который, находясь в составе эритроцитов, связывает кислород. Последний, в свою очередь, несется к мышцам, а там передает кислород другому белку — миоглобину. Гемоглобин и миоглобин — это первые два белка, для которых были определены трехмерные структуры, расшифрованные методом рентгеноструктурного анализа, за что Перуцу и Кендрью была вручена Нобелевская премия.
Есть еще каталитическая функция, которая осуществляется при помощи специальных белков — ферментов. Они катализируют какую-либо реакцию. Так, фермент алкогольдегидрогеназа, как можно догадаться из названия, расщепляет алкоголь. Соединительной функцией занимается, например, коллаген — белок, составляющий основу соединительной ткани организма (сухожилий, костей, хрящей). Существуют у белков и другие задачи. В целом можно сказать так: в нашем организме более 20 тысяч генов. И почти все из них — гены, кодирующие белки. Это о многом говорит.
Существуют у белков и другие задачи. В целом можно сказать так: в нашем организме более 20 тысяч генов. И почти все из них — гены, кодирующие белки. Это о многом говорит.
— Что интересного сегодня происходит в науке о белках?
— Очень своевременный вопрос: если бы вы задали его до лета 2018 года, то мой ответ был бы совершенно другим. Что у нас случилось? Прорыв! Немного предыстории. В 1961 году было экспериментально показано, что трехмерная форма белка, о которой мы говорили, определяется исключительно аминокислотной последовательностью (до этого думали, что в этом играют роль рибосомы). А в 1969 году это подтвердилось окончательно, когда без участия рибосомы химически синтезировали полностью функциональный белок. Поэтому ученые рассудили: если мы знаем аминокислотную последовательность — мы можем предсказать и трехмерную структуру белка. Но на деле все оказалось не так просто.
В итоге прошло полвека непрерывных попыток — частичных успехов и разочарований. И вот, в 2018 году компания DeepMind, которая принадлежит Google, представила уникальную программу AlphaFold по предсказанию трехмерной структуры белка. Интересно, что «разминались» они на создании программ по игре в шахматы и го, у которых похожий принцип — обучаться на примере удачных и неудачных ходов, которые ведут то к победе, то к поражению. Шахматная программа стала умной до такой степени, что за шесть часов тренировки при определенном количестве процессоров оказалась способна обыграть любого человека в мире.
Интересно, что «разминались» они на создании программ по игре в шахматы и го, у которых похожий принцип — обучаться на примере удачных и неудачных ходов, которые ведут то к победе, то к поражению. Шахматная программа стала умной до такой степени, что за шесть часов тренировки при определенном количестве процессоров оказалась способна обыграть любого человека в мире.
И в 2020 году путем тренировок AlphaFold добилась другого успеха — в предсказаниях структуры белков. Точность таковых — от 88% до 90%, почти как в экспериментах. Это очень хороший результат. И теперь любой желающий может установить эту программу и получить возможность предсказывать трехмерные структуры практически с экспериментальной точностью. А может зайти в базу данных моделей AlphaFold, и найти структуру любого известного белка .
— И что нам это дает?
— Очень многое. Ведь зная трехмерную структуру белка, мы можем узнать и о его функции. Сегодня на планете свирепствует коронавирус. Известно, что он зацепляется за клетку хозяина при помощи так называемого шипикового (спайкового) белка, о котором было много шума и публикаций. Теперь мы знаем его структуру, что дает нам возможность борьбы с этим вирусом. И не только с ним, но и с другими заболеваниями. Этот успех может облегчить поиск нужных лекарств, разработку новых вакцин и антибиотиков.
Теперь мы знаем его структуру, что дает нам возможность борьбы с этим вирусом. И не только с ним, но и с другими заболеваниями. Этот успех может облегчить поиск нужных лекарств, разработку новых вакцин и антибиотиков.
Кроме того, это будет способствовать прогрессу в создании белков с заданными свойствами. Сфера применения таковых не ограничивается биологией и медициной. Взять ту же промышленность, где уже сегодня белки используют в качестве биодобавок в стиральных порошках — там они играют роль тех самых «умных молекул», о которых нам рассказывает реклама. Есть сладкие на вкус белки, которые могут служить безопасными заменителями сахара.
— Над чем конкретно работаете вы?
— Мне как раз очень интересна тема структуры белка и ее изменений. Дело в том, что при внесении «мутаций» в белки мы можем добиться улучшения необходимых нам свойств. Например, можно сделать белки более устойчивыми к высокой температуре или уровню pH. Над этим сейчас и работает наша лаборатория. А вообще хочется добиться экспертизы уровня группы Дэвида Бейкера (знаменитого американского биохимика и компьютерного биолога, который впервые разработал методы прогнозирования и проектирования трехмерных структур белков — прим. авт.), директора Института белкового дизайна, который и создали специально в результате его успехов. Он, конечно, берется за очень серьезные задачи — например, с нуля создает белок, которые светится каким-нибудь цветом. А в конце 2000-х его команда сгенерировала белок, катализирующий реакцию, которая не существует в природе. Так что есть мечта — добиться похожих результатов.
А вообще хочется добиться экспертизы уровня группы Дэвида Бейкера (знаменитого американского биохимика и компьютерного биолога, который впервые разработал методы прогнозирования и проектирования трехмерных структур белков — прим. авт.), директора Института белкового дизайна, который и создали специально в результате его успехов. Он, конечно, берется за очень серьезные задачи — например, с нуля создает белок, которые светится каким-нибудь цветом. А в конце 2000-х его команда сгенерировала белок, катализирующий реакцию, которая не существует в природе. Так что есть мечта — добиться похожих результатов.
Дмитрий Иванков на семинаре. Источник: Тимур Сабиров
— Кстати, как вы вообще пришли в биологию?
— Вы знаете, в школе мне была интересна вовсе не биология, а физика и математика. И после одной из олимпиад учительница физики перетянула меня в физмат класс. А после этого, на выпускном, сагитировала поступить в МФТИ и убедила в этом моих родителей, за что я ей и моим родителям очень благодарен. Я поступил также на физфак в МГУ, но выбрал МФТИ и пошел на тот факультет, куда всегда хотел — радиотехники и кибернетики. На кафедру системного программирования — как раз к тому коллективу авторов, который создал отечественный суперкомпьютер.
Я поступил также на физфак в МГУ, но выбрал МФТИ и пошел на тот факультет, куда всегда хотел — радиотехники и кибернетики. На кафедру системного программирования — как раз к тому коллективу авторов, который создал отечественный суперкомпьютер.
И тут один мой друг случайно рассказал мне об Институте белка РАН. Он сообщил, что Алексей Витальевич Финкельштейн — в дальнейшем мой первый научный руководитель, член-корреспондент Российской академии наук и совершенно замечательный человек и ученый, возглавляющий в Пущино Лабораторию физики белка, — ищет студента для выполнения задачи. Я тогда пообещал своему другу приехать, а у самого мысли: «Какая ерунда, где я — и где белки?». Я тогда даже не знал, что такое белки! Но приехал.
Оказалось, там очень интересный сегмент работы, и Алексей Витальевич меня сразу принял. А потом выяснилось, что мне даже не надо переводиться на другой факультет. Так я и учился на кафедре системного программирования, сочиняя для диплома программу про сворачивание белков. На защите рассказывал, что такое белки, как они сворачиваются. Одним очень понравилось, другие, наоборот, были недовольны тем, что их отвлекают от работы по проектированию микропроцессоров и системного программирования всякой ерундой. После этого я пошел стажером-исследователем, а затем аспирантом в Институт белка и проработал там до конца 2009 года, после чего продолжил работать за границей.
На защите рассказывал, что такое белки, как они сворачиваются. Одним очень понравилось, другие, наоборот, были недовольны тем, что их отвлекают от работы по проектированию микропроцессоров и системного программирования всякой ерундой. После этого я пошел стажером-исследователем, а затем аспирантом в Институт белка и проработал там до конца 2009 года, после чего продолжил работать за границей.
Знаете, в академической среде есть принцип — нужно менять место работы и браться за новые проекты. Потому что чем больше таких мест работы в CV, тем богаче у тебя опыт. Да мне вообще казалось, что в моей области никаких глобальных вопросов уже нет, поэтому я поехал за рубеж — узнать, что происходит в соседних областях науки. Сначала четыре года поработал постдоком в Германии в Техническом университете Мюнхена у профессора Дмитрия Фришмана, потом четыре года в Барселоне у другого профессора — Федора Кондрашова. Потом вся лаборатория Федора переехала в Австрию, и я вместе с ней.
— Как вам помог такой разносторонний опыт общения с коллегами?
— Расширением работы моей лаборатории. Потому что одно ее направление — это изучение структуры белков, а второе — эволюция, исследование эпистаза (типа взаимодействия генов между собой — прим. авт.). Последний вектор возник благодаря тому, что я работал в Лаборатории эволюционной геномики у Федора Кондрашова. Я уже не говорю о том, что международный опыт значительно расширяет круг интересов, старые знания сочетаются с новыми. Поэтому чем старше исследователь, тем шире его кругозор, тем более зрел и целостен его взгляд на науку.
Потому что одно ее направление — это изучение структуры белков, а второе — эволюция, исследование эпистаза (типа взаимодействия генов между собой — прим. авт.). Последний вектор возник благодаря тому, что я работал в Лаборатории эволюционной геномики у Федора Кондрашова. Я уже не говорю о том, что международный опыт значительно расширяет круг интересов, старые знания сочетаются с новыми. Поэтому чем старше исследователь, тем шире его кругозор, тем более зрел и целостен его взгляд на науку.
Теги
Интервью
График работы черной белки
Покрытие СВ, СД, ОК, МО, КС и ИА
| Январь 2022 | Местоположение | Результаты | ||
|---|---|---|---|---|
| 1/23 | Молодежный открытый чемпионат Северо-Западного Миссури # 1 | Мэривилл, Миссури, | ||
| Февраль 2022 | Местоположение | Результаты | ||
| 2/19 | Топика Super Indoor Invitational Записи закрыты | Топика, Канзас | ||
| апрель 2022 | Местоположение | Результаты | ||
| 4/1 | Чепмен Приглашение | Чепмен, Канзас | ||
| 4/15 | Трэвис Шили (Нью-Гэмпшир) Invitational | Аллен, Канзас | ||
| 4/18 | Приглашение на лигу MCAA | Топика, Канзас | ||
| 4/30 | Чемпионат конференции KCI | Гауэр, Миссури, | ||
| 4/30 | Приглашение на лигу MCAA | Топика, Канзас | ||
| май 2022 | Местоположение | Результаты | ||
| 5/12 | Столетняя лига Записи закрыты | Эмпория, Канзас | ||
| 5/19 | 6A Региональный 3 — Топика Хай Записи закрыты | Топика, Канзас | ||
| 5/19 | 2A Региональный 18 — Линдон Записи закрыты | Линдон, Канзас | ||
| 5/20 | 3A Regional 15 — Долина Хойт-Ройал Записи закрыты | Хойт, Канзас | ||
| 5/20 | 5A Региональный 6 — Эмпория Записи закрыты | Эмпория, Канзас | ||
| Сентябрь 2022 | Местоположение | Результаты | ||
| 9/3 | Мэрисвилл XC Пригласить Записи закрыты | Мэрисвилл, Канзас | ||
| 17 сентября | Одесса XC Invite Записи закрыты | Одесса, МО | ||
| 22 сентября | Приглашение на юго-восток по пересеченной местности Записи закрыты | Чероки, Канзас | ||
| 28 сентября | Дубовая роща Записи закрыты | Дубовая роща, Миссури | ||
| Октябрь 2022 | Местоположение | Результаты | ||
| 10/1 | Приглашение моряка Записи закрыты | Топика, Канзас | ||
| 10/8 | Wichita Trinity — фестиваль дикого ветра Записи закрыты | Уичито, Канзас | ||
| 10/8 | Межвузовское приглашение Great Plains | Макферсон, Канзас | ||
| 10/15 | Маранафа Инвайт Записи закрыты | Олате, Канзас | ||
| 10/15 | KC Suburban Золотая / Серебряная конференция Записи закрыты | Саммит Ли, Миссури | ||
22. 10. 10. | KSHSAA 4A Regional — Топика-Хайден Записи закрыты | Топика, Канзас | ||
| 22.10. | KSHSAA 1A Regional — округ Вашингтон Записи закрыты | Вашингтон, штат Канзас, | ||
22. 10. 10. | KSHSAA 2A Regional — Ричмонд-Центральные высоты Записи закрыты | Ричмонд, Канзас | ||
| 22.10. | KSHSAA 2A, региональный — Вабаунзее Записи закрыты | Алма, Канзас | ||
22. 10. 10. | КШСАА 5А Региональный — Топика Западная Записи закрыты | Топика, Канзас | ||
| 29.10 | MSHSAA Класс 3 — Район 4 Онлайн запись | Платт-Сити, Миссури, | ||
29. 10 10 | MSHSAA Класс 2 — Район 4 Онлайн запись | Платт-Сити, Миссури, | ||
| 29.10 | MSHSAA Класс 1 — Район 4 Онлайн запись | Платт-Сити, Миссури, | ||
Angry Squirrel — Masters, Am 1, Am 3, Am Masters 50+ и 60+, Юниоры
MA1 · Advanced (21)
Joel Coppernoll #45151
Professional
Spring Arbor, Michigan, United States
Кертис Лафонд № 56552
Любительское
Холт, Мичиган, США
Адам Макферсон #83046
Профессиональный
Кантон, Мичиган, США
Tyler Schoening #81703
Professional
Анн-Арбор, Мичиган, США
Brock Way #37380
Professional
East Lansing, Michigan, United States
Кевин Квятковски #41252
Профессиональный
Детройт, Мичиган, США
Энтони Льюис #43979
Любитель
Ричленд, Мичиган, США
Майкл Уолтерс #61780
Любитель
Дженисон, Мичиган, США
Эрик Ньютон #96630
Любитель
Альто, Мичиган, США
Chris Laity #71765
Любитель
New Baltimore, Michigan, United States
Wyatt Vandybogurt #92524
Любитель
Колдуотер, Мичиган, США
Zachary Colosimo #57710
Любитель
Farmingtn Hls, Мичиган, США
Тайлер Альфано #70266
Любительское
Sterling Hts, Мичиган, США
Zachary Malott #77161
Любитель
Скоттвилл, Мичиган, США
Джастин Гроу #89201
Любитель
Хортон, Мичиган, США
Джордж Штурм #23933
Любитель
Маунт Клеменс, Мичиган, США
Тайлер Берг #72013
Любитель
Гранд-Рапидс, Мичиган, США
Брайс Харрелл #
Любитель
Хортон, Мичиган, США
Томас Миковски #22005
Профессиональный
Брайтон, Мичиган, США
Парк Победы — Длинные тройники; 18 отверстий; пар.
